Notícias
Fosfoetanolamina: realidade, promessa ou mais um pesadelo?
Fonte: Cemed - Centro de Estudos do Medicamento
Data de publicação: 23 de outubro de 2015
Créditos: Joyce Costa Melgaço de Faria
O Centro de Estudos do Medicamento (Cemed) recebeu uma consulta sobre a fosfoetanolamina e por entendermos que se trata de uma dúvida gerada pela forte exposição dessa substância na mídia, julgamos conveniente oferecer alguns esclarecimentos à população.
Fosfoetanolamina em foco
Fosfoetanolamina em foco
A fosfoetanolamina sintética está em evidência na mídia por ser uma suposta alternativa inovadora para o tratamento do câncer. Ela chegou a ter sua produção e fornecimento proibidos, porém voltou a ser produzida para atender a uma liminar concedida pelo STF (Supremo Tribunal Federal) 1. Mas por que essa decisão é controversa? Quais as razões éticas e legais para impedir as pessoas que sofrem com o câncer de utilizarem uma substância que aparentemente traz resultados benéficos? A resposta para essas perguntas envolve o entendimento de um longo processo de pesquisa, segmentado em várias etapas, que se inicia com a descoberta de uma nova substância e vai até o registro de um medicamento inovador pelas agências de regulação sanitária. Embora a primeira vista possa parecer uma burocracia cruel, na verdade o rigor para a liberação de uma substância no mercado é uma necessidade de controle para proteger a população de um mal maior.
Fases para o desenvolvimento de um medicamento: o caso da fosfoetanolamina
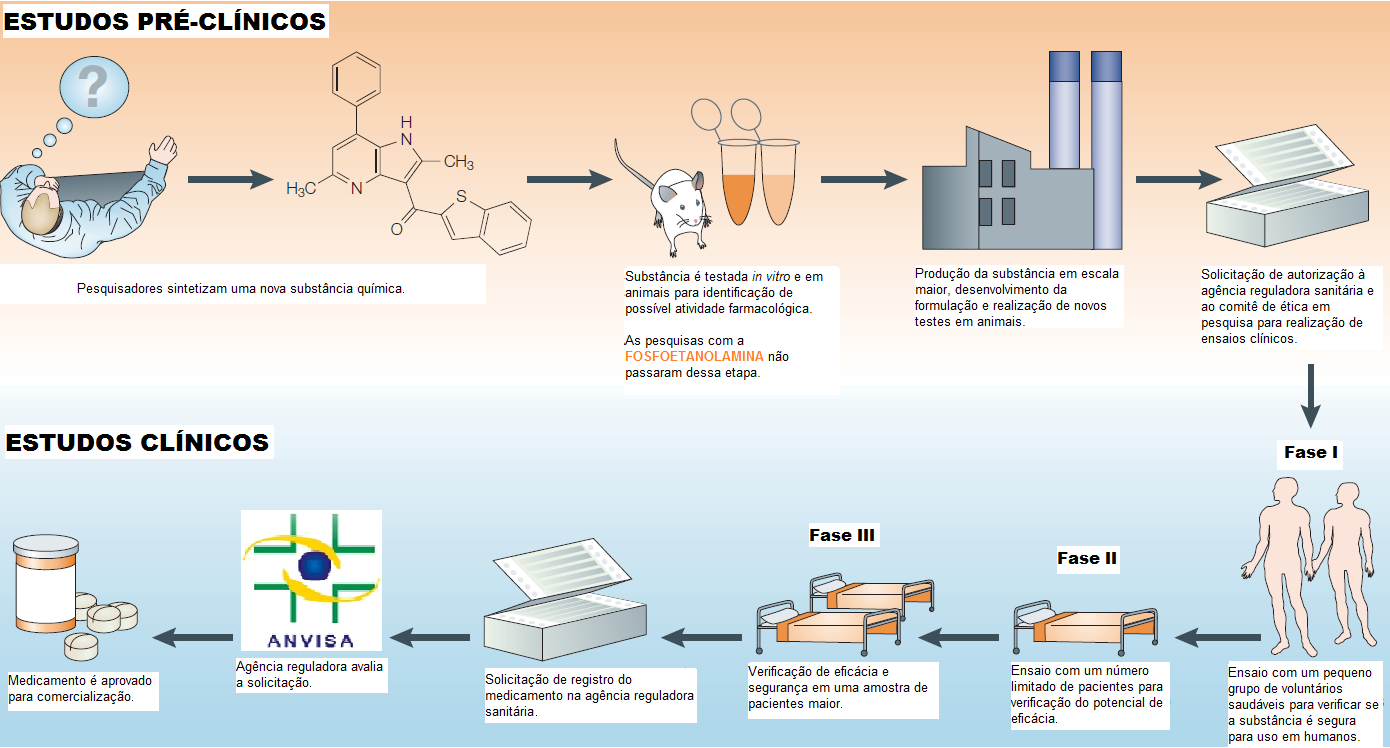
Fases do desenvolvimento de um novo medicamento (clique para ampliar). Fonte: adaptado de Lombardino e Lowe (2004) (2)
A fase mais avançada nas pesquisas de desenvolvimento de um novo medicamento é denominada fase clínica, quando são feitos testes em seres humanos para comprovar se o medicamento é eficaz e se seus efeitos adversos são toleráveis (ensaios clínicos controlados). Esses ensaios são complexos, e condicionados à existência de uma série de pesquisas prévias sobre o fármaco. Eles demandam tempo, recursos humanos e financeiros, planejamento e um grande número de participantes voluntários. Para saber mais sobre a fase clínica recomendamos a leitura do texto “Como os seres humanos participam da fase clínica das pesquisas sobre medicamentos”, publicado pelo Cemed.
A fosfoetanolamina é apenas mais uma substância candidata a medicamento. As pesquisas com essa substância ainda estão nas fases preliminares do longo processo de desenvolvimento de novos medicamentos. Embora elas ocorram há mais de uma década, somente testes in vitro (cultura de células) e em animais foram realizados até o momento 3,4,5,6,7, e esses são insuficientes para comprovar sua eficácia e segurança em seres humanos. Muitas substâncias apresentam resultados satisfatórios nos experimentos in vitro ou em animais, mas não obtêm sucesso quando utilizadas por humanos, podendo causar danos à saúde (não nos esqueçamos da talidomida e do sofrimento que causou )8. Estima-se que apenas nove a cada vinte mil substâncias testadas na fase pré-clínica se tornam medicamento, e apenas uma entre essas nove tem real utilidade no mercado farmacêutico 9.
Há relatos de pessoas que utilizaram a fosfoetanolamina e se “curaram” do câncer. No entanto, esses relatos isolados têm pouco ou nenhum valor científico, uma vez que não são bem conhecidas as características dos pacientes e da doença tratada, as condições em que a substância foi usada, qual a dose e frequência de administração e nem se outros medicamentos estavam sendo utilizados concomitantemente. Não podemos nos esquecer de que essas curas não necessariamente se deram por causa da substância. Para se ter certeza sobre isso é preciso que pesquisas científicas sejam realizadas.
A saúde baseada em evidências é requisito para tomada de decisão
A recomendação de uso de substâncias que não têm comprovação de eficácia e segurança por profissionais fere princípios éticos e expõe a população a riscos que ela, diferente desses profissionais, não consegue dimensionar. E, ainda, diverge dos princípios da prática de saúde baseada em evidências. A medicina baseada em evidências (MBE) é o uso consciente, explícito e criterioso das melhores evidências científicas disponíveis para tomar decisões em relação ao manejo de pacientes. A prática da MBE consiste na integração da expertise clínica do profissional com as evidências de maior qualidade provenientes da pesquisa sistemática 10.
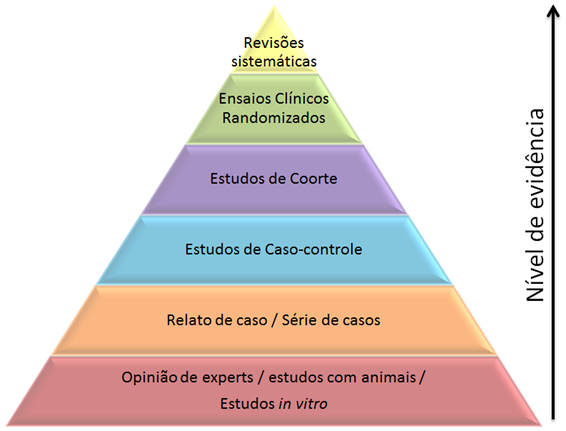
A Pirâmide da Evidência é uma proposta utilizada na MBE para classificar os estudos científicos de acordo com o nível de evidência, isto é, o poder que cada metodologia de pesquisa tem de responder questões da prática clínica. No topo desta pirâmide estão as revisões sistemáticas, estudos em que os dados de um conjunto de ensaios clínicos são agregados de forma sistemática para garantir maior qualidade à evidência gerada. Embora um ensaio clínico bem elaborado seja suficiente para a aprovação de um novo medicamento, a revisão sistemática é considerada a melhor evidência para tomada de decisões em saúde, pois reúne informações de vários deles 11.
Observa-se que os ensaios clínicos estão próximos ao topo da pirâmide, ao passo que os estudos in vitro, os estudos com animais e os relatos de caso encontram-se na base. Portanto, as pesquisas que até então foram realizadas com a fosfoetanolamina estão muito aquém do necessário para sustentar sua utilização como medicamento. A ilustração da pirâmide demonstra a lacuna existente entre os resultados de pesquisa que podem ser imediatamente aplicados na prática clínica e os que não podem. Os estudos de coorte e os de caso-controle não tem aplicabilidade direta na aprovação de um novo medicamento, mas podem ser úteis na identificação de reações adversas de medicamentos já comercializados e serem determinantes na retirada de um medicamento do mercado.
Fosfoetanolamina: longa trajetória até tornar-se um medicamento para tratar o câncer
Muitas pessoas aguardam ansiosas por novos tratamentos para o câncer e várias outras doenças. Entretanto, não é coerente a utilização de substâncias cujos efeitos em humanos ainda não são bem conhecidos, uma vez que o risco do uso pode superar os benefícios. Além disso, a própria USP (Universidade de São Paulo) admite que seus padrões de produção da fosfoetanolamina são artesanais e não atendem aos requisitos exigidos para a produção de um medicamento. As agências reguladoras sanitárias devem zelar pela segurança da população, garantindo que estejam disponíveis no mercado apenas medicamentos cuja eficácia, segurança e qualidade já foram comprovadas. As exigências da Anvisa (Agência Nacional de Vigilância Sanitária) não são mera burocracia associada a interesses econômicos. São medidas importantes para evitar que a saúde das pessoas seja prejudicada com o uso de substâncias de procedência, qualidade e utilidade duvidosas. O Poder Judiciário deve levar isso em consideração ao julgar o direito legítimo das pessoas à vida e ao tratamento de seus males.
Referências:
1 Supremo Tribunal Federal. Liminar garante a uma paciente fornecimento de substância pela USP-São Carlos Internet. Brasília; 2015 out 8. acesso em 2015 out 21. Disponível em: http://www.stf.jus.br/portal/cms/verNoticiaDetalhe.asp?idConteudo=301441
2 Lombardino JG, Lowe JA. The role of the medicinal chemist in drug discovery — Thennow. Nat Rev Drug Discov. 2004 out; 3(10):853-62.
3 Ferreira AK, Santana-Lemos BAA , Rego EM, Filho OMR , Chierice GO, Maria DA. Synthetic phosphoethanolamine has in vitroin vivo anti-leukemia effects. Br J Cancer. 2013 nov 7. 109(11):2819-28.
4 Ferreira AK, Meneguelo R, Pereira A, Filho, OMR, Chierice GO, Maria, DA. Synthetic phosphoethanolamine induces cell cycle arrestapoptosis in human breast cancer MCF-7 cells through the mitochondrial pathway. Biomed Pharmacother. 2013 jul. 67(6):481-7.
5 Ferreira AK, Freitas VM, Levy D, Ruiz JL, Bydlowski SP, Rici RE, Filho OM, Chierice GO, Maria DA. Anti-angiogenicanti-metastatic activity of synthetic phosphoethanolamine. PLoS One. 2013 mar; 8(3):e57937.
6 Ferreira AK, Meneguelo R, Pereira A, Filho, OMR, Chierice GO, Maria, DA. Anticancer Effects of Synthetic Phosphoethanolamine on Ehrlich Ascites Tumor: An Experimental Study. Anticancer Res. 2012; 32(1): 95-104.
7 Ferreira AK, Meneguelo R, Marques FL, Radin A, Filho OM, Neto SC, Chierice GO, Maria DA. Synthetic Phosphoethanolamine a precursor of membrane phospholipids reduce tumor growth in mice bearing melanoma B16-F10in vitro induce apoptosisarrest in G2/M phase. Biomed Pharmacother. 2012; 66(7):541-8.
8 Fuchs FD, Wannmacher L. Farmacologia Clínica. Fundamentos da Terapêutica Racional. 4 ed. Rio de Janeiro: Editora Guanabara Koogan; 2010. Capítulo 1.
9 Calixto JB, Siqueira Jr JM. Desenvolvimento de Medicamentos no Brasil: Desafios. Gaz. Méd. Bahia. 2008; 78(Suplemento 1):98-106.
10 Sackett DL, Rosenberg WM, Gray JA, Haynes RB, Richardson WS. Evidence based medicine: what it iswhat it isn’t. BMJ. 1996 jan 13; 312(7023):71-2.
11 Chiappelli F; Brant XMC; Negoita N; Oluwadara OO; Ramchandani MH, editores. Evidence-Based Practice: Toward Optimizing Clinical Outcomes. Berlin: Springer; 2010